
สำหรับนักเรียนที่กำลังเตรียมตัวสอบวิชาวิทยาศาสตร์และเคมี เรื่อง “ธาตุและตารางธาตุ” คือหัวใจสำคัญที่ออกสอบทุกสนาม ไม่ว่าจะเป็นสอบกลางภาค, ปลายภาค หรือสอบเข้ามหาวิทยาลัย (A-Level / TGAT) แต่เนื้อหาธาตุมีมหาศาล จะจำทั้งหมดคงไม่ไหว
บทความนี้จึงรวบรวมเฉพาะ “จุดเน้น” และ “คุณสมบัติของธาตุที่ออกสอบบ่อยที่สุด” พร้อมทริคการจำและตารางสรุปที่จะช่วยให้คุณทำข้อสอบได้อย่างมั่นใจครับ
1. พื้นฐานตารางธาตุที่ต้องแม่น

ก่อนจะไปดูคุณสมบัติ ต้องเข้าใจโครงสร้างของตารางธาตุก่อน เพราะข้อสอบมักจะถามถึงความสัมพันธ์ของตำแหน่งธาตุ
- หมู่ (Group): แถวในแนวตั้ง (มี 18 หมู่) – ธาตุในหมู่เดียวกันจะมี “สมบัติทางเคมีคล้ายกัน” เพราะมีจำนวนเวเลนซ์อิเล็กตรอน (Valence Electron) เท่ากัน
- คาบ (Period): แถวในแนวนอน (มี 7 คาบ) – ธาตุในคาบเดียวกันจะมี “จำนวนระดับชั้นพลังงานเท่ากัน”
จุดที่ออกสอบบ่อย: ข้อสอบมักถามว่า “ธาตุ X อยู่หมู่ 2 คาบ 3 จะมีสมบัติคล้ายธาตุใด” คำตอบคือต้องหาธาตุที่อยู่หมู่ 2 เหมือนกันนั่นเองครับ
2. การแบ่งกลุ่มธาตุตามสมบัติ (Metals, Non-metals, Metalloids)
ข้อสอบมักจะให้คุณสมบัติมา แล้วถามว่าเป็นธาตุประเภทใด หรือให้เปรียบเทียบความแตกต่าง
โลหะ (Metals)
- คุณสมบัติ: ผิวมันวาว, นำไฟฟ้าและนำความร้อนได้ดีมาก, จุดเดือดจุดหลอมเหลวสูง, ตีเป็นแผ่นหรือดึงเป็นเส้นได้, สถานะส่วนใหญ่เป็นของแข็ง (ยกเว้น ปรอท Hg ที่เป็นของเหลว)
- ตำแหน่ง: อยู่ทางซ้ายและกลางของตารางธาตุ
อโลหะ (Non-metals)
- คุณสมบัติ: ไม่มันวาว, ไม่นำไฟฟ้า (ยกเว้น กราไฟต์), จุดเดือดจุดหลอมเหลวต่ำ, เปราะหักง่าย, มีทั้ง 3 สถานะ (ของแข็ง, ของเหลว, ก๊าซ)
- ตำแหน่ง: อยู่ทางขวาของตารางธาตุ
กึ่งโลหะ (Metalloids)
- คุณสมบัติ: มีสมบัติกึ่งกลางระหว่างโลหะและอโลหะ เช่น นำไฟฟ้าได้บ้างแต่ไม่ดีเท่าโลหะ (สารกึ่งตัวนำ)
- ธาตุเด่น: โบรอน (B), ซิลิคอน (Si), เจอร์เมเนียม (Ge)
3. กลุ่มธาตุ “ตัวตึง” ที่ออกสอบบ่อยที่สุด

มี 4 กลุ่มหลักที่คุณต้องจำสมบัติให้ขึ้นใจ เพราะออกข้อสอบแทบทุกปี:
1. หมู่ 1A: โลหะแอลคาไล (Alkali Metals)
- ธาตุเด่น: Li, Na, K
- จุดเด่น: ว่องไวต่อการเกิดปฏิกิริยาสูงมาก (โดยเฉพาะกับน้ำจะเกิดก๊าซไฮโดรเจน H2 และสารละลายเป็นเบส), อ่อนนุ่ม ตัดได้ด้วยมีด
2. หมู่ 2A: โลหะแอลคาไลน์เอิร์ท (Alkaline Earth Metals)
- ธาตุเด่น: Be, Mg, Ca
- จุดเด่น: ว่องไวต่อปฏิกิริยา (แต่น้อยกว่าหมู่ 1), พบมากในธรรมชาติในรูปของแร่ธาตุและหินปูน
3. หมู่ 7A: แฮโลเจน (Halogens)
- ธาตุเด่น: F, Cl, Br, I
- จุดเด่น: อโลหะที่ว่องไวต่อปฏิกิริยาสูงที่สุด, มักทำปฏิกิริยากับโลหะเกิดเป็นเกลือ (Halide), มีสถานะครบทั้ง 3 ในหมู่เดียว
4. หมู่ 8A: ก๊าซเฉื่อย (Noble Gases)
- ธาตุเด่น: He, Ne, Ar, Kr
- จุดเด่น: เสถียรมาก ไม่ทำปฏิกิริยากับใคร (เพราะมีอิเล็กตรอนเต็มวง), ใช้เติมในหลอดไฟหรือบอลลูน
4. แนวโน้มสมบัติตามตารางธาตุ (Periodic Trends)
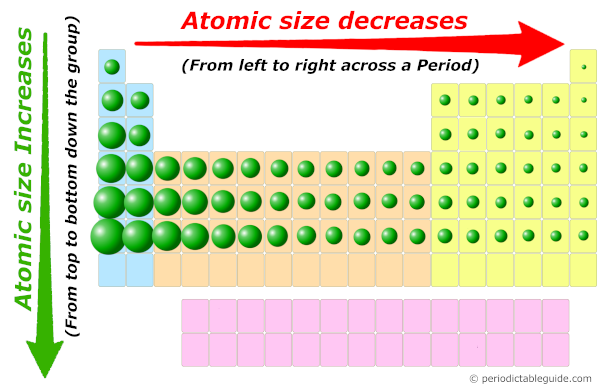
ส่วนนี้คือจุดที่นักเรียนพลาดบ่อยที่สุด ให้จำ “ทิศทาง” ของการเปลี่ยนแปลงดังนี้ครับ:
| สมบัติ | ตามหมู่ (บน ไป ล่าง) | ตามคาบ (ซ้าย ไป ขวา) | ทริคการจำ |
|---|---|---|---|
| ขนาดอะตอม | ใหญ่ขึ้น | เล็กลง | ลงล่างชั้นพลังงานเพิ่ม -> ใหญ่ขึ้น / ไปขวาประจุบวกดึงดูดมากขึ้น -> เล็กลง |
| ค่า IE (พลังงานไอออไนเซชัน) | ลดลง | เพิ่มขึ้น | อะตอมใหญ่ดึงอิเล็กตรอนยาก -> IE ต่ำ |
| ค่า EN (ความสามารถในการดึง e-) | ลดลง | เพิ่มขึ้น | ขวาสุด (F) หิวอิเล็กตรอนที่สุด -> EN สูงสุด |
| ความเป็นโลหะ | เพิ่มขึ้น | ลดลง | ด้านซ้ายล่างคือ “ที่สุดของโลหะ” |
5. สรุปทริคทำข้อสอบ: จุดที่มักโดนหลอก
- อย่าลืม “ข้อยกเว้น”: เช่น ปรอท (Hg) เป็นโลหะแต่เป็นของเหลว, กราไฟต์เป็นอโลหะแต่นำไฟฟ้าได้
- ระวังเรื่องขนาด: ข้อสอบมักถามเปรียบเทียบ เช่น “ธาตุ Na กับ K ใครใหญ่กว่ากัน” -> ให้ดูว่าใครอยู่ล่างกว่า (K อยู่ล่างกว่า Na ดังนั้น K ใหญ่กว่า)
- ความสัมพันธ์ IE และ EN: จำไว้ว่า “ขนาดอะตอม” คือตัวกำหนด ถ้าอะตอมเล็ก -> จะดึงอิเล็กตรอนเก่ง (EN สูง) และดึงอิเล็กตรอนออกยาก (IE สูง)
คำถามที่พบบ่อย (FAQ)
Q: ทำไมธาตุหมู่ 8 ถึงไม่ทำปฏิกิริยากับธาตุอื่น
A: เพราะมีอิเล็กตรอนวงนอกสุดเต็มตามกฎออกเตต (Octet Rule) ทำให้มีความเสถียรสูงสุด ไม่จำเป็นต้องรับหรือจ่ายอิเล็กตรอนให้กับใคร
Q: ค่า EN (Electronegativity) สูงสุดคือธาตุอะไร
A: ฟลูออรีน (F) เป็นธาตุที่มีค่า EN สูงที่สุดในตารางธาตุ
Q: อยากได้คะแนนเต็มเรื่องตารางธาตุ ต้องเน้นจุดไหน
A: เน้นเรื่อง แนวโน้มสมบัติ (Periodic Trends) และ สมบัติเฉพาะของหมู่ 1, 2, 7, 8 เพราะเป็นจุดที่ใช้ทดสอบความเข้าใจได้ดีที่สุด

ใส่ความเห็น