
วิชาเคมีจะกลายเป็นเรื่องง่ายทันที ถ้าคุณเข้าใจหัวใจสำคัญอย่าง “โครงสร้างอะตอม” (Atomic Structure) และ “ตารางธาตุ” (Periodic Table) เพราะนี่คือพื้นฐานของสสารทุกครับ
บทความนี้จะสรุปเนื้อหาที่ต้องรู้ ตั้งแต่ส่วนประกอบของอะตอม วิวัฒนาการแบบจำลอง ไปจนถึงเทคนิคการดูแนวโน้มในตารางธาตุกันครับ
อะตอมคืออะไร เจาะลึกโครงสร้างพื้นฐาน

อะตอม (Atom) คือ หน่วยที่เล็กที่สุดของธาตุที่ยังคงแสดงคุณสมบัติของธาตุนั้นๆ ได้ ประกอบด้วยอนุภาคมูลฐาน 3 ชนิด ได้แก่:
- โปรตอน (Proton, p+): มีประจุบวก อยู่ในนิวเคลียส (ใจกลางอะตอม)
- นิวตรอน (Neutron, n): เป็นกลางทางไฟฟ้า อยู่ในนิวเคลียสรวมกับโปรตอน
- อิเล็กตรอน (Electron, e–): มีประจุลบ วิ่งวนรอบนิวเคลียสด้วยความเร็วสูง มีมวลน้อยมากๆ จนแทบไม่นับรวมในน้ำหนักอะตอม
Note: ในอะตอมที่เป็นกลางทางไฟฟ้า จำนวน โปรตอน จะเท่ากับ อิเล็กตรอน เสมอ
วิวัฒนาการของ “แบบจำลองอะตอม”
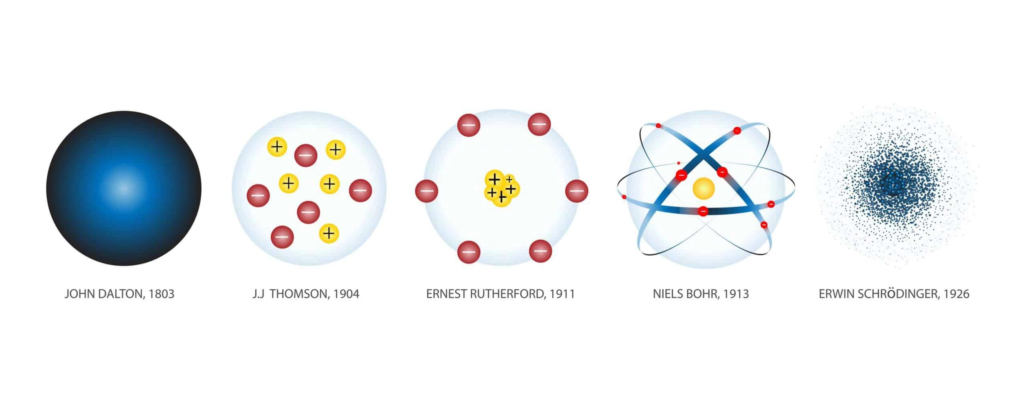
กว่าเราจะรูปร่างหน้าตาของอะตอมในปัจจุบัน นักวิทยาศาสตร์ได้เสนอแนวคิดและทดลองมาหลายยุคสมัย สรุปสั้นๆ ได้ดังนี้:
- ดอลตัน (Dalton): ทรงกลมตัน แบ่งแยกไม่ได้ (เหมือนลูกบิลเลียด)
- ทอมสัน (Thomson): ทรงกลมบวก มีอิเล็กตรอนลบฝังอยู่ (เหมือนแตงโมมีเมล็ด)
- รัทเทอร์ฟอร์ด (Rutherford): มีนิวเคลียส (บวก) อยู่ตรงกลาง อิเล็กตรอนวิ่งรอบๆ พื้นที่ส่วนใหญ่เป็นที่ว่าง
- โบร์ (Bohr): อิเล็กตรอนวิ่งรอบนิวเคลียสเป็นชั้นๆ หรือ “ระดับพลังงาน” (เหมือนวงโคจรดาวเคราะห์)
- แบบกลุ่มหมอก (Electron Cloud): อิเล็กตรอนเคลื่อนที่เร็วมากจนระบุตำแหน่งไม่ได้ บอกได้แค่ “โอกาสที่จะพบ” ซึ่งบริเวณใกล้นิวเคลียสจะมีโอกาสพบมากที่สุด (เป็นแบบจำลองที่ยอมรับในปัจจุบัน)
สัญลักษณ์นิวเคลียร์: รหัสลับบอกตัวตนธาตุ
สัญลักษณ์นิวเคลียร์ (Nuclear Symbol) คือการเขียนสัญลักษณ์เพื่อบอกจำนวนอนุภาคในอะตอม โดยมีรูปแบบดังนี้:
AZ X
- X: สัญลักษณ์ของธาตุ (เช่น C, H, O)
- A (เลขมวล): คือ โปรตอน + นิวตรอน (น้ำหนักของอะตอม)
- Z (เลขอะตอม): คือ จำนวน โปรตอน (ซึ่งเท่ากับอิเล็กตรอนในภาวะเป็นกลาง) เป็นเลขบัตรประชาชนของธาตุ เปลี่ยนไม่ได้
ตัวอย่าง: คาร์บอน-12 (126C)
- มีโปรตอน = 6
- มีอิเล็กตรอน = 6
- มีนิวตรอน = 12 – 6 = 6
ตารางธาตุ (Periodic Table): แผนที่ของนักเคมี

ตารางธาตุคือการจัดระเบียบธาตุต่างๆ ตาม “เลขอะตอม” และ “สมบัติที่คล้ายคลึงกัน”
โครงสร้างหลักของตารางธาตุ
- หมู่ (Group): แถวแนวตั้ง มีทั้งหมด 18 หมู่ (หลักๆ ที่เรียนคือหมู่ 1A – 8A) ธาตุในหมู่เดียวกันจะมี เวเลนซ์อิเล็กตรอน (Valence Electron) เท่ากัน ทำให้มีสมบัติทางเคมีคล้ายกัน
- หมู่ 1: โลหะอัลคาไล (ว่องไวต่อปฏิกิริยามาก)
- หมู่ 7: แฮโลเจน (ก๊าซพิษ สารฆ่าเชื้อ)
- หมู่ 8: ก๊าซเฉื่อย (ไม่ค่อยทำปฏิกิริยากับใคร)
- คาบ (Period): แถวแนวนอน มี 7 คาบ บอกถึงจำนวน “ระดับพลังงาน” (วงโคจร) ของอิเล็กตรอน
แนวโน้มตารางธาตุ
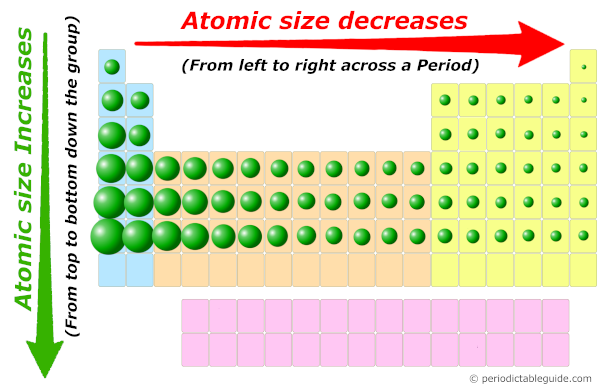
นี่คือหัวใจสำคัญที่มักออกสอบ! การรู้ตำแหน่งในตารางธาตุ ช่วยให้เราทำนายสมบัติของธาตุนั้นได้
A. ขนาดอะตอม (Atomic Radius)
- จากบนลงล่าง (หมู่เดียวกัน): ขนาด ใหญ่ขึ้น (เพราะมีระดับพลังงานชั้นเพิ่มขึ้น)
- จากซ้ายไปขวา (คาบเดียวกัน): ขนาด เล็กลง (เพราะโปรตอนในนิวเคลียสเยอะขึ้น ดึงดูดอิเล็กตรอนเข้ามาใกล้ตัวได้แรงขึ้น)
B. ค่า EN (Electronegativity)
คือ ความสามารถในการดึงดูดอิเล็กตรอน (ความหวงอิเล็กตรอน)
- ธาตุฟลูออรีน (F): เป็นตัวแม่! มีค่า EN สูงที่สุดในตารางธาตุ (อยู่ขวาบน)
- แนวโน้ม: ตรงข้ามกับขนาดอะตอม ยิ่งตัวเล็ก ยิ่งดึงดูดเก่ง (ขวาบน EN สูง / ซ้ายล่าง EN ต่ำ)
C. พลังงานไอออไนเซชัน (IE)
คือ พลังงานที่ใช้ดึงอิเล็กตรอนให้หลุดออกจากอะตอม
- พวก ก๊าซเฉื่อย (หมู่ 8) จะมีค่า IE สูงมาก เพราะมันเสถียรแล้ว ไม่อยากให้อิเล็กตรอนใคร
- พวก โลหะ (หมู่ 1) มีค่า IE ต่ำ ดึงออกง่ายมาก จึงชอบกลายเป็นประจุบวก

ใส่ความเห็น